
Sobre o Estudo NoVa
O estudo NoVa é um ensaio clínico aberto, multicêntrico, controlado e randomizado de iniciativa do investigador. É mais uma parceria entre o Instituto de Pesquisa do Hcor e a BRICNet (Rede Brasileira de Pesquisa em Terapia Intensiva). O Estudo NoVa compara a efetividade do uso de vasopressina precoce versus noradrenalina e vasopressina de resgate em pacientes com sepse dependente de vasopressores.
Nossa hipótese é que o uso de vasopressina precoce pode estar associado a uma redução na mortalidade e na necessidade de terapia substitutiva renal (TSR).
Para testar essa hipótese, planejamos incluir 2800 pacientes com sepse dependente de vasopressores em UTIs de todo o Brasil.
Clinicaltrials.gov: NCT06464510
Sua UTI tem interesse em participar do estudo? Se sim, clique no botão abaixo:
Racional do Estudo: Uso de Vasopressina no Tratamento da Sepse
A sepse é uma condição grave definida como uma disfunção orgânica ameaçadora à vida, causada por uma resposta desregulada do corpo a uma infecção. Nos casos mais graves, como o choque séptico, há alterações circulatórias e metabólicas profundas, que aumentam significativamente o risco de morte.
Em 2017, foram registrados cerca de 48,9 milhões de casos de sepse no mundo, resultando em 11 milhões de mortes — o que representa 19,7% de todas as mortes globais. No Brasil, dados indicam que 30% dos leitos de UTI são ocupados por pacientes com sepse, com uma mortalidade que supera 50% entre os pacientes com choque séptico.1
Para o tratamento da sepse, o guia da Campanha Sobrevivendo à Sepse recomenda o diagnóstico precoce, intervenções rápidas, como reposição volêmica para pacientes com disfunção hemodinâmica, e a administração precoce de antibióticos. Um dos pilares desse tratamento é a ressuscitação hemodinâmica com cristaloides intravenosos e o uso de vasopressores em casos de hipotensão.2
Atualmente, a noradrenalina é o vasopressor de escolha no tratamento da hipotensão em pacientes sépticos. No entanto, seu uso pode estar associado a efeitos colaterais importantes, como arritmias cardíacas, alterações imunológicas, de coagulação e metabólicas.3-12
A vasopressina, um hormônio produzido naturalmente pelo organismo, surge como uma alternativa à noradrenalina. Ela age como um potente vasoconstritor ao se ligar ao receptor V1a, presente nas células musculares lisas dos vasos sanguíneos. Além disso, a vasopressina pode trazer benefícios, como o aumento da pressão de perfusão renal.13
O racional deste estudo é baseado na ideia de usar a vasopressina de forma precoce em um dos grupos de pacientes, expondo-os a menores doses e menor tempo de uso da noradrenalina, o que pode reduzir os efeitos colaterais associados a este medicamento. Ao mesmo tempo, esses pacientes receberão vasopressina por um período maior, explorando seus potenciais efeitos benéficos, como a melhora da perfusão renal.
População
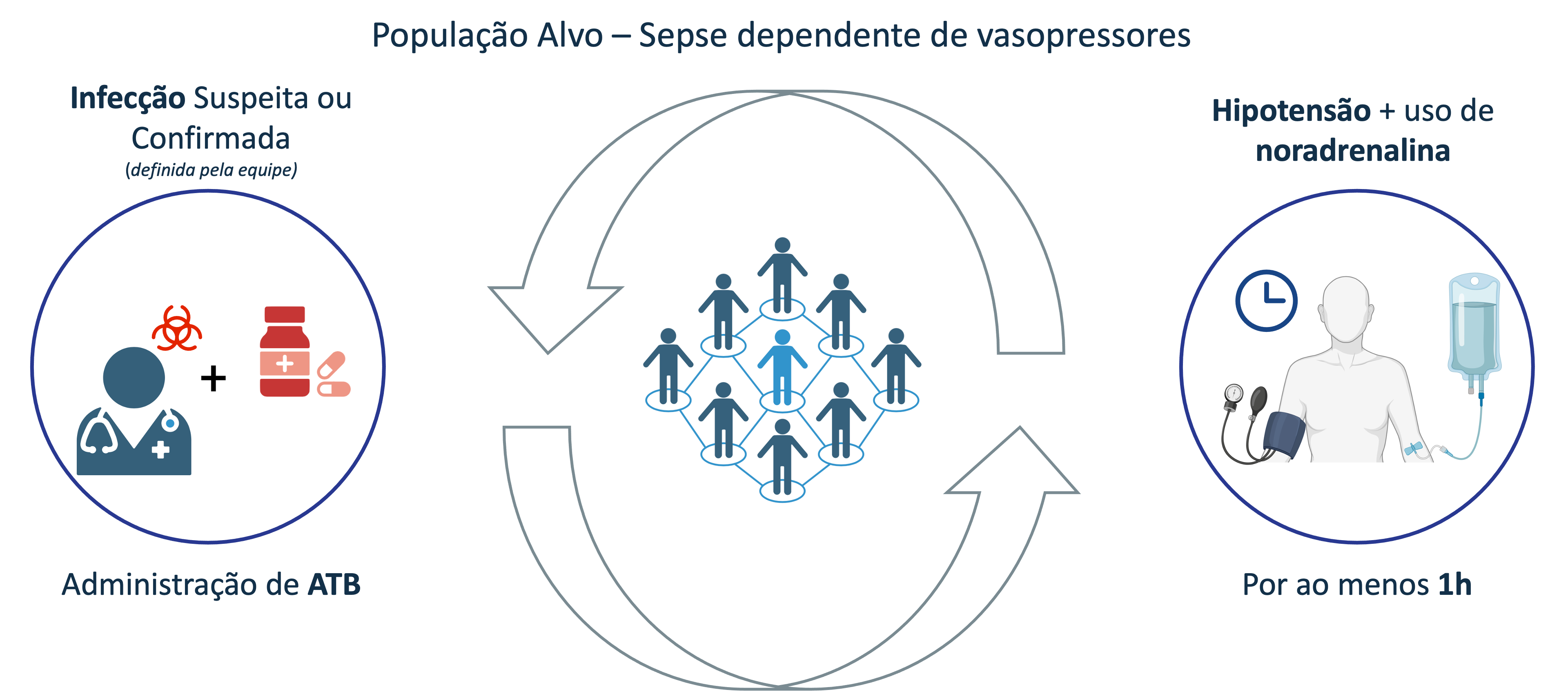
Critérios de Inclusão
- Adultos (≥18 anos)
- Internados em UTI ou com previsão de admissão em UTI nas
- próximas 12 horas
- Ressuscitação volêmica adequada
- Sepse dependente de vasopressores
- Uso de noradrenalina > 0.05μg/Kg/min e ≤ 0.25μg/Kg/min por ao menos 1 hora e no máximo 24 horas no momento da inclusão
Critérios de Exclusão
- Uso de noradrenalina > 0.25μg/Kg/min nas últimas 24 horas, exceto se administrada transitoriamente no contexto de sedação para procedimento ou fase inicial de ressuscitação volêmica por período menor que uma hora
- Doença renal crônica dialítica ou lesão renal aguda que receberam terapia substitutiva renal na internação ou são esperados receber terapia substitutiva renal nas próximas 24 horas
- Uso de outros vasopressores que não noradrenalina
- Uso de vasopressores para sepse nos últimos 7 dias
- Isquemia mesentérica aguda suspeita ou confirmada
- Anafilaxia ou hipersensibilidade conhecida a droga do estudo
- Perspectiva de óbito em menos de 24 horas
- Equipe médica não comprometida a investimento pleno no momento da inclusão
- Inclusão prévia no estudo
Intervenções
Grupo Vasopressina Precoce
Vasopressina na dose de 0.01UI/min (3ml/h) a 0.04UI/min (12ml/h) após a randomização, objetivando a manutenção da PAm alvo. A manutenção ou aumento da noradrenalina poderá ocorrer somente após a titulação vasopressina tiver atingido sua dose máxima (0.04UI/min) e o paciente com PAm abaixo do alvo. Poderá ocorrer situações em que o único vasopressor em uso será a vasopressina.
Grupo Vasopressina de Resgate
Vasopressina será iniciada somente quando participante atingir dose de noradrenalina >0.5μg/Kg/min. Nesse momento, terá início a infusão de vasopressina na dose de 0.01UI/min (3ml/h) que poderá ser titulada até a dose máxima de 0.04UI/min (12ml/h) para atingir a PAm alvo.
Desfechos
Desfecho primário composto de mortalidade por todas as causas ou terapia substitutiva renal em 28 dias. A hipótese principal é que a associação precoce de vasopressina reduz o desfecho composto em pacientes com sepse dependente de vasopressores internados em UTI.
Patrocinador e Financiador
O Hcor e a BRICNet possuem total controle independente sobre o estudo e são os únicos responsáveis por sua condução. O Hcor, dessa forma, assume também a responsabilidade como patrocinador do estudo, em conformidade com as regulamentações aplicáveis.
A Biolab Sanus Farmacêutica Ltda (Brasil) fornecerá a vasopressina (Encrise®) utilizada no estudo, além de oferecer apoio financeiro ao patrocinador. Vale destacar que a Biolab Sanus Farmacêutica Ltda não terá acesso a dados que possam identificar pacientes individualmente, não participará do desenvolvimento do protocolo, não influenciará decisões relacionadas ao andamento do estudo, nem estará envolvida na decisão de publicação dos resultados.
Referencias
- Machado FR, Cavalcanti AB, Bozza FA, et al. The epidemiology of sepsis in Brazilian intensive care units (the Sepsis PREvalence Assessment Database, SPREAD): an observational study. The Lancet Infectious Diseases 2017;17(11):1180-1189. DOI: 10.1016/S1473-3099(17)30322-5.
- Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med 2021;47(11):1181-1247. (In eng). DOI: 10.1007/s00134-021-06506-y.
- Stolk RF, van der Poll T, Angus DC, van der Hoeven JG, Pickkers P, Kox M. Potentially Inadvertent Immunomodulation: Norepinephrine Use in Sepsis. Am J Respir Crit Care Med 2016;194(5):550-8. DOI: 10.1164/rccm.201604-0862CP.
- Wenisch C, Parschalk B, Weiss A, et al. High-dose catecholamine treatment decreases polymorphonuclear leukocyte phagocytic capacity and reactive oxygen production. Clin Diagn Lab Immunol 1996;3(4):423-8. DOI: 10.1128/cdli.3.4.423-428.1996.
- van der Poll T, Jansen J, Endert E, Sauerwein HP, van Deventer SJ. Noradrenaline inhibits lipopolysaccharide-induced tumor necrosis factor and interleukin 6 production in human whole blood. Infect Immun 1994;62(5):2046-50. DOI: 10.1128/iai.62.5.2046-2050.1994.
- Huang HW, Tang JL, Han XH, Peng YP, Qiu YH. Lymphocyte-derived catecholamines induce a shift of Th1/Th2 balance toward Th2 polarization. Neuroimmunomodulation 2013;20(1):1-8. DOI: 10.1159/000343099.
- Ramer-Quinn DS, Baker RA, Sanders VM. Activated T helper 1 and T helper 2 cells differentially express the beta-2-adrenergic receptor: a mechanism for selective modulation of T helper 1 cell cytokine production. J Immunol 1997;159(10):4857-67. (https://www.ncbi.nlm.nih.gov/pubmed/9366411).
- Lyte M, Freestone PP, Neal CP, et al. Stimulation of Staphylococcus epidermidis growth and biofilm formation by catecholamine inotropes. Lancet 2003;361(9352):130-5. DOI: 10.1016/S0140-6736(03)12231-3.
- Sandrini S, Alghofaili F, Freestone P, Yesilkaya H. Host stress hormone norepinephrine stimulates pneumococcal growth, biofilm formation and virulence gene expression. BMC Microbiol 2014;14:180. DOI: 10.1186/1471-2180-14-180.
- von Kanel R, Dimsdale JE. Effects of sympathetic activation by adrenergic infusions on hemostasis in vivo. Eur J Haematol 2000;65(6):357-69. DOI: 10.1034/j.1600-0609.2000.065006357.x.
Adeva-Andany M, Lopez-Ojen M, Funcasta-Calderon R, et al. - Comprehensive review on lactate metabolism in human health. Mitochondrion 2014;17:76-100. DOI: 10.1016/j.mito.2014.05.007.
- Rizza RA, Cryer PE, Haymond MW, Gerich JE. Adrenergic mechanisms of catecholamine action on glucose homeostasis in man. Metabolism 1980;29(11 Suppl 1):1155-63. DOI: 10.1016/0026-0495(80)90025-6.
- Russell JA. Bench-to-bedside review: Vasopressin in the management of septic shock. Crit Care 2011;15(4):226. (In eng). DOI: 10.1186/cc8224.



